Negli ultimi 50 anni nel settore farmaceutico si è iniziato ad assistere ad un fenomeno allarmante: a fronte di un aumento esponenziale degli investimenti in ricerca, il numero di nuovi farmaci sviluppati e portati ai pazienti diminuiva.
E’ la legge di Eroom, ossia l’esatto contrario della legge di Moore secondo la quale invece nel mondo dell’elettronica e dell’informatica «La complessità di un microcircuito, misurata ad esempio tramite il numero di transistor per chip, raddoppia ogni 18 mesi (e quadruplica quindi ogni 3 anni).»
In pratica se nell’elettronica ad ogni aumento degli investimenti corrisponde un incremento logaritmico dello sviluppo tecnologico nel mondo farmaceutico sta avvenendo l’esatto contrario.
Immaginate per un attimo di essere alla guida di un’azienda che vende biscotti e di accorgervi che nonostante ogni anno aumentiate gli investimenti in pubblicità il numero di confezioni vendute cali costantemente. Cosa fareste?
Potrebbe esserci qualche direttore marketing che vi convinca a temporeggiare, “è un periodo particolare per tutto il settore – vi potrebbe dire – se continuiamo ad investire riusciamo ad uscirne salvi e conquistare anche il mercato della concorrenza”. Altri potrebbero dirvi “è normale, per vedere risultati sulle vendite bisogna avere pazienza, ma dobbiamo continuare a investire altrimenti chissà quanto ancora meno venderemmo” O altre argomentazioni simili. Quale sia la decisione giusta da prendere è difficile da sapere ma una cosa è certa: il tempo ed i risultati forniranno la risposta.
La crisi della ricerca nel settore farmaceutico
Sono passati più di 50 anni e nonostante i vostri costanti investimenti in pubblicità continuate a vendere sempre meno biscotti.
Questo è ciò che in qualche maniera sta avvenendo nel settore della ricerca e sviluppo farmaceutico, ovviamente con i dovuti distinguo del caso.
Osservate questo grafico pubblicato su Nature, rappresenta il numero di nuovi farmaci immessi in commercio per ogni miliardo di dollaro investito.
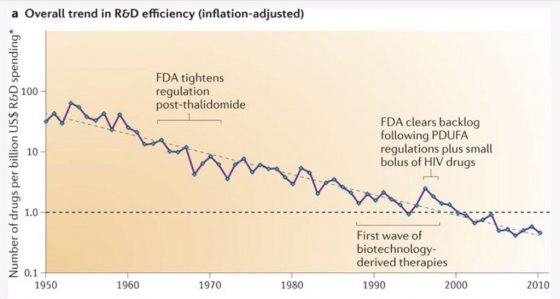
Il trend parla chiaro: se negli anni 50 per ogni miliardo di dollari investito si sviluppavano una media di 50-60 nuovi farmaci all’anno, nel 2010 per ogni miliardo di dollaro investito non si riesce a sviluppare nemmeno un singolo nuovo farmaco. Il tutto ovviamente considerando la variazione del valore del dollaro negli anni.
Eppure in questi decenni sono state messe a punto tecniche di ricerca e sviluppo sempre più efficienti. Prendiamo ad esempio il cosiddetto high-throughput screening (o screening ad alto rendimento). E’ il metodo più utilizzato per cercare nuove molecole con il potenziale di diventare futuri farmaci, un metodo che si basa sulla robotica, sull’analisi computazionale, sui Big Data, sull’Intelligenza Artificiale, etc.. un metodo che ogni anno viene perfezionato e reso sempre più efficiente grazie all’innovazione tecnologica e che fondamentalmente garantisce ai ricercatori la possibilità di analizzare e testare velocemente centinaia di migliaia di molecole su altrettanti possibili recettori e strutture biologiche.
Bene, nonostante tutta questa efficienza il numero di nuovi farmaci scoperti cala costantemente. Non solo, spesso i nuovi farmaci sviluppati sono efficaci solo su una piccola percentuale di pazienti, vale pertanto la pena nobilitarli chiamandoli “farmaci personalizzati”.
Paradossalmente sarebbe più efficiente e meno costoso esplorare a piedi la foresta amazzonica alla ricerca di nuove piante dal potenziale terapeutico.
Quali sono le ragioni di questa crisi?
Jack Scannell e colleghi, gli autori di questo studio pubblicato su Nature e che peraltro lavorano per la Sanford C. Bernstein Limited, una grossa società finanziaria internazionale che si occupa di investimenti in ricerca, hanno identificato quattro fattori che stanno alla base di questa crisi:
- il fattore “meglio di uno scarafaggio”, che qui in Italia qualcuno potrebbe storpiare trasformandolo in “ogni scarrafone è bello a mamma sua”. Al di là delle battute con quest’espressione gli autori indicano il fatto che oggi stia diventando sempre più difficile sviluppare farmaci realmente innovativi e più efficaci di quelli già esistenti. Quello che si riesce a fare sono solo piccoli miglioramenti dei farmaci già presenti sul mercato. E’ difficile trovare nuove classi di farmaci con nuovi meccanismi d’azione. Sembra che il “grosso” sia già stato scoperto e sviluppato e così ci si deve accontentare di piccolissime differenze, a volte minime anche se confrontate con lo stesso placebo.
- Il progressivo irrigidimento delle procedure di registrazione dei farmaci: qui gli autori evidenziano il fatto che le agenzie regolatorie dei farmaci per tutelare i pazienti dai rischi di possibili effetti indesiderati abbiamo alzato di molto le richieste sui requisiti per poter accettare e registrare nuovi farmaci. Questo obbliga le aziende a spendere molto di più per poter fornire tutte le documentazioni richieste.
- Una tendenza a sprecare le risorse finanziarie: per molto tempo, anche a causa dei grossi profitti delle aziende farmaceutiche, l’abitudine ad un’oculata gestione del budget di ricerca è stata poco presa in considerazione e di conseguenza gli sprechi ancora oggi sono molti.
- Troppa fiducia negli attuali modelli di ricerca di base: Scannell e colleghi spiegano che i ricercatori hanno riposto troppa fiducia nelle potenzialità delle metodiche di high-throughput screening che poi come visto per il momento hanno portato a risultati scarsi rispetto alle aspettative.
Forse la ricerca ha bisogno di ripensare a sé stessa
C’è un quinto punto, che forse potrebbe essere il più importante di tutti: probabilmente l’impostazione generale della ricerca moderna va ripensata facendola evolvere.
Da anni numerosi ricercatori, ciascuno dal punto di vista della sua specifica specializzazione, affermano che sia necessario sviluppare una “nuova teoria della biologia”, un “nuovo paradigma”.
Come spiega il prof. Mariano Bizzarri “la conoscenza scientifica non è qualcosa di assoluto e dato per sempre ma è un processo in continua evoluzione. Il modo con cui noi pensiamo e modelliamo la realtà determina il tipo di esperimenti che facciamo, il tipo di dati che ne ricaviamo finanche al nostro modo di interpretarli”.
E’ necessario pertanto definire il quadro epistemologico all’interno del quale ci stiamo muovendo identificandone i limiti entro i quali tale visione è in grado di spiegare i fenomeni osservati.
La storia della scienza ci ha dimostrato come certi approcci possano risultare fertili anche per centinaia di anni ma poi, come spiega lo storico e filosofo della scienza Thomas Kuhn, a un certo punto la cosiddetta “scienza normale” smette di essere efficiente cedendo il passo alle rivoluzioni scientifiche che avvengono proprio perché qualcuno ha il coraggio di cambiare il quadro epistemologico con cui si guarda e si sperimenta la natura avviando un vero e proprio cambio di paradigma.
Forse ora è tempo che avvenga una nuova “rivoluzione scientifica” nel modo con cui facciamo ricerca sui nuovi farmaci.
Fonti:
-
Scannell JW., Blanckley A., Boldon H., Warrington, B. – Diagnosing the decline in pharmaceutical R&D efficiency, Nature Reviews Drug Discovery, Volume 11, (191-200) 2012 (https://www.nature.com/articles/nrd3681)
-
Lowe D. – Eroom’s Law – Science Translational Medicine (https://blogs.sciencemag.org/pipeline/archives/2012/03/08/erooms_law)
-
Bizzarri, M, 2018, “There is something rotten in the state of the Pharma Industry”, Organisms. Journal of Biological Sciences, vol. 2, no. 1, pp. 11-13 ( https://ojs.uniroma1.it/index.php/Organisms/article/view/14341/14045 )
-
Kuhn T. – The Structure of Scientific Revolutions, University of Chicago Press (1962)
Ultimi post di Andrea Pensotti (vedi tutti)
- Così riduciamo dell’80% le ospedalizzazioni per COVID-19 - Aprile 21, 2021
- Il traduttore simultaneo che “parla” direttamente al cervello grazie alla trasmissione ossea del suono - Giugno 5, 2020
- Microchip sottocutanei e social rating saranno presto realtà? - Maggio 28, 2020